 In der Welt der menschlichen Wirtschaft, Politik, und Gesellschaft, Es gibt viele verschiedene Währungen, die alle gegen Waren gehandelt werden. Das könnte Öl sein, US Dollar, Facebook likes oder Omas Cookies. Die natürliche Welt hat ähnliche Währungen – der Handel mit Sauerstoff, Kohlenstoff, und vielleicht die wertvollste Währung von allen: Stickstoff- .
In der Welt der menschlichen Wirtschaft, Politik, und Gesellschaft, Es gibt viele verschiedene Währungen, die alle gegen Waren gehandelt werden. Das könnte Öl sein, US Dollar, Facebook likes oder Omas Cookies. Die natürliche Welt hat ähnliche Währungen – der Handel mit Sauerstoff, Kohlenstoff, und vielleicht die wertvollste Währung von allen: Stickstoff- .
Die ganze Welt kämpft dafür, ehrlich ernten, betrügen dafür, und stehlen es brutal. Es ist ein starkes Element, in höchsten Mengen für gutes Wachstum benötigt, Verteidigung, und Reproduktion. Dieser Artikel behandelt, was Stickstoff ist, wo es im System vorkommt, und wie es mit den anderen Elementen der Aquaponik interagiert. Wir werden auch besprechen, wie man einen Stickstoffmangel erkennt.
Wie ich bereits erwähnt habe, Stickstoff ist einer der wichtigsten Nährstoffe in Ihrem Aquaponik-System. Es kommt in verschiedenen Formen in der Natur vor, aber für den Moment, Wir werden uns auf das relevanteste konzentrieren:Protein.
Protein besteht aus Aminosäuren, die selbst aus Stickstoff aufgebaut sind. Alle Pflanzen und Tiere enthalten Proteine, und wenn sie sterben, andere Organismen verbrauchen sie und sammeln diese Proteine für Energie. Daher, Stickstoff gelangt in Form von eiweißhaltiger Nahrung in den Körper.
Wenn Landtiere Proteine konsumieren, zerlegen sie diese schließlich in Aminosäuren und dann in Ammoniak. Ammoniak (NH3) ist ein unangenehmes Zeug – es ist sehr giftig – und der beste Weg, überschüssiges Ammoniak loszuwerden, besteht darin, es auszuscheiden. So, bei Landtieren, Ammoniak wird in eine Chemikalie namens Harnstoff umgewandelt und mit dem Urin ausgeschieden.
Stickstoff kommt in aquaponischen Systemen auf ähnliche Weise vor. Es tritt in Form von Fischfutter auf. Die Fische verzehren das Futter, aber der Vorgang ist einfacher; Die Mikroben in ihren Bäuchen bauen die Proteine zu Ammoniak und Ammonium ab. Ammoniak liegt normalerweise als Ammonium (NH4+) vor, das sich durch die Zellmembranen der Fische bewegt und schließlich ins Wasser diffundiert. Keine zusätzliche Konvertierung notwendig. Für Fische, ohnehin.
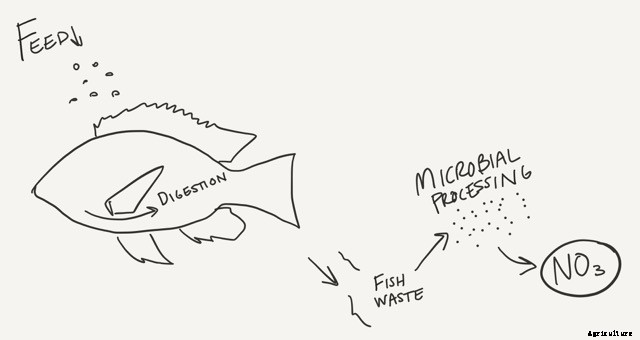
Abhängig vom pH-Wert Ihres Wassers, Ammonium kann Ammonium bleiben oder sich in Ammoniak verwandeln, was sehr gefährlich sein kann. Ammoniak hat keine Ladung, Daher haben die Fische Schwierigkeiten, es aus ihrem Körper herauszuhalten. Wenn das passiert, die fische sind vergiftet.
So, Sobald Ammoniak in der Lösung ist, es muss umgewandelt werden oder es wird schließlich den Fisch töten. Es gibt zwei Möglichkeiten, dies zu tun:Ändern Sie Ihren pH-Wert, um Ammonium zu bevorzugen (was nicht empfohlen wird) oder wandeln Sie das Ammoniak in Nitrate um. Die Reihe der Umwandlungen von einer organischen Form (Ammoniak) in eine pflanzenverfügbare Form (Nitrat) – und der nächste Schritt im Zyklus – heißt Nitrifikation.
Nitrifikation ist der Prozess, der die meisten Aquaponik-Systeme antreibt. Im Wesentlichen, Nitrifikation wandelt Ammoniak und Ammonium in nützliches Nitrat um. Dies geschieht in zwei Prozessen:Umwandlung von Ammoniak in Nitrit, und Umwandlung von Nitrit in Nitrat.
In fast allen Umgebungen (außer anaeroben Umgebungen) wird Ammoniak schnell in . umgewandelt Nitrit (NO2-). Mikroben – oder nitrifizierende Bakterien —im Boden oder in der Lösung Sauerstoff zu (oder oxidieren ) das Ammoniak. Während dies geschieht, die Mikroben erhalten die Energie, um Kohlenstoff zu fixieren (Kohlenstoff aus Kohlendioxid brechen, um Zellen aufzubauen). Zusätzlich, Es entstehen Wasserstoffionen (H+) – genau die Ionen, die beim pH-Test gemessen werden und das Wasser sauer werden lassen.
Dieser Vorgang wird traditionell einem Bakterium namens Nitrosomonas zugeschrieben. Neuere Forschungen zeigen, dass es viele Hundert, wenn nicht Tausende von verschiedenen Arten zusätzlich zu Nitrosomonas die machen auch diese arbeit.
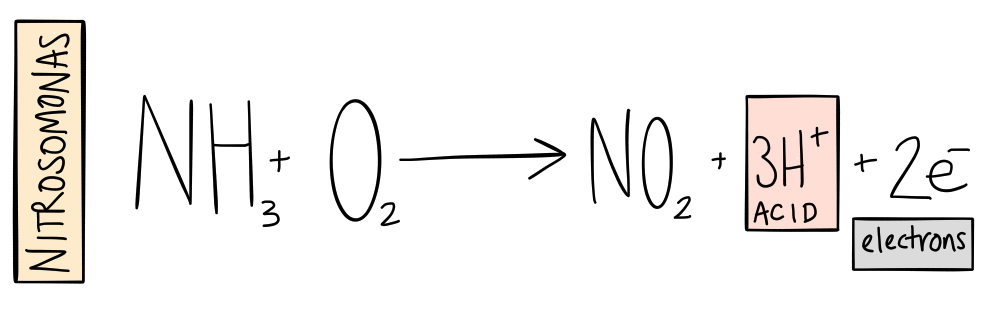
Das ist Schritt eins.
Der nächste Schritt im Zyklus besteht darin, dieses Nitrit in Nitrat umzuwandeln. Nitrit ist auch ziemlich giftig, sodass Sie nie zu viel in Ihrem System haben möchten. Glücklicherweise, es repräsentiert viel gespeicherte Energie für andere [nitrifizierende] Bakterien. Diese Bakterien oxidieren das Nitrit und nutzen die Energie aus dem Prozess, um mehr Kohlenstoff zu binden. Klingt vertraut, außer dieses Mal ist das Ergebnis Nitrat (NR. 3-). Nitrat ist eine relativ ungiftige Form von Stickstoff, die Pflanzen aufnehmen und zum Aufbau von Zellen verwenden können.
Das Bakterium, das am häufigsten für die Durchführung dieser chemischen Reaktion bekannt ist, wird Nitrobacter genannt. Wieder, jedoch, Untersuchungen zeigen, dass neben Nitrobacter viele Bakterien an dieser Reaktion beteiligt sind.
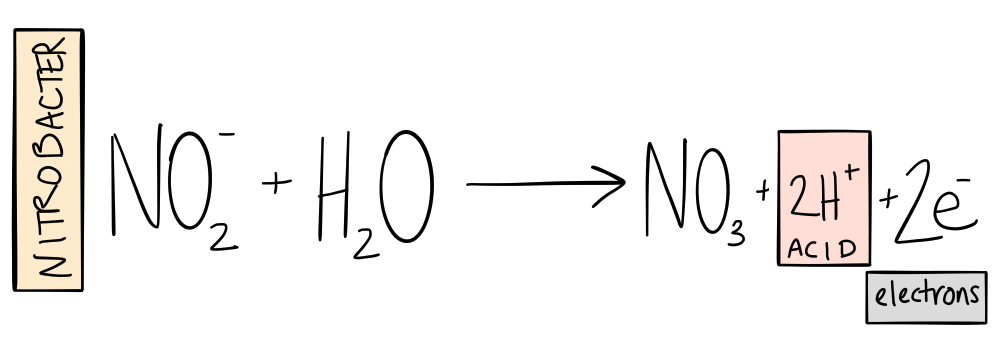
Da die Bakterien Ammoniak und Nitrit oxidieren, sie geben Hydroniumionen in die Lösung ab, macht das System saurer. (Für Personen, die ihre Systeme im optimalen pH-Bereich für die Nährstoffverfügbarkeit betreiben möchten, Nitrifikation ist der wichtigste Prozess zur Senkung des pH-Wertes). Dies deutet darauf hin, warum die Lösung älterer Systeme zu saureren pH-Werten tendiert.
Stickstoff ist bei einer Vielzahl von pH-Werten verfügbar – der pH-Wert spielt also keine Rolle, wenn es um die Stickstoffverfügbarkeit geht.
„… die Nitrifikation ist der wichtigste Prozess zur Senkung des pH-Werts.“
Die Geschwindigkeit, mit der sich der pH-Wert einer Lösung ändert, jedoch, können die verfügbare Stickstoffform (siehe Video zu Ammoniak/Ammonium und pH) sowie die Effizienz der Nitrifikation beeinflussen. Wenn nitrifizierenden Bakterien keine Zeit gegeben wird, sich an sich ändernde pH-Werte anzupassen (wie fast jede andere Systemvariable), die Nitrifikation leidet.
Eigentlich, Die Nitrifikation verläuft bei niedrigen pH-Werten gut, solange der nitrifizierenden Ökologie Zeit zur Anpassung gegeben wird. Nitrifizierende Bakterien sind im Allgemeinen ineffizient, wenn es um die Änderung von Systemvariablen geht. Sie sterben oft ab oder ruhen, wenn sie zu viel Licht ausgesetzt sind. Temperaturschwankungen, Schwankungen des Salzgehalts und des pH-Werts, sowie viele andere Veränderungen in ihrer Umgebung.
Das wahrgenommene Gleichgewicht zwischen pH-Wert und Nitrifikationseffizienz basiert auf der Annahme, dass die Nitrifikationsaktivität in aquaponischen Systemen hauptsächlich von zwei verschiedenen Bakteriengruppen abhängt: Nitrosomonas spp., und Nitrobacter spp.
In Laborversuchen, diese Bakterienarten haben eine Empfindlichkeit gegenüber dem pH-Wert gezeigt, mit pH-Änderungen, die ihre Fähigkeit beeinträchtigen, Ammoniak (Nitrosomonas) und Nitrit (Nitrobacter) zu oxidieren. Denken Sie daran, dass die meisten nitrifizierenden Bakterien (zumindest bisher untersucht) nicht gut mit sich ändernden Umgebungsvariablen umgehen. Dies ist aus zwei Gründen wichtig zu wissen:
Was hat das mit der Nitrifikationsdebatte zu tun? Brunnen, Punkt 1 sagt uns, dass vielleicht viele der „Systemabstürze“, die einem zu niedrigen pH-Wert des Systems zugeschrieben werden, tatsächlich auf eine zu schnelle Senkung des pH-Werts des Systems zurückzuführen sind. Punkt 2 sagt uns, dass Nitrosomonas und Nitrobacter möglicherweise nicht wirklich die Richtigen sind die meisten wichtige Nitrifizierer in Systemen – sie sind einfach die am einfachsten zu isolierenden und in einer Petrischale im Labor anzubauenden Gruppen.
Es bedeutet im Grunde, dass die festen Regeln der Nitrifikation möglicherweise nicht so hart und schnell sind, wie sie normalerweise kommuniziert werden. Es gibt viele Systeme, die in sehr niedrigen pH-Bereichen mit hoher Nitrifikationseffizienz arbeiten (einschließlich unseres). Es kann sein, dass Nitrosomonas und Nitrobacter-Spezies die primären Nitrifizierer in unserem System sind, aber die Realität ist, dass wir es einfach nicht wissen. Was wir wissen ist, dass unsere Nitrifikation unabhängig von unserem System-pH-Wert effizient und ausgezeichnet ist.
Um dies ins rechte Licht zu rücken, Es gibt viele saure Böden und Meeresumgebungen auf der ganzen Welt, in denen die Nitrifikation bei bemerkenswert niedrigen pH-Bereichen stattfindet. Viele der Nitrifisatoren in diesen Umgebungen gehören nicht zu den Gruppen Nitrobacter oder Nitrosomonas. Viele von ihnen sind unbekannt. In einer einzigen Schaufel Erde, Es gibt schätzungsweise 10, 000 verschiedene Bakterienarten oder etwa doppelt so viele Bakterien, die der Wissenschaft derzeit bekannt sind.
In diesem Sinne, Ich denke, es ist nicht nur möglich, aber wahrscheinlich gibt es einige ziemlich interessante Bakterien, die nitrifizierende Funktionen in aquaponischen Systemen auf der ganzen Welt erfüllen.
Sehen Sie sich unser BSA-Video an, in dem die biologische Oberfläche detailliert beschrieben wird – das wohl wichtigste Systemdesignelement, das die Nitrifikation fördert.
 Auf jeden Fall, das Endprodukt ist Nitrat (NO3-). Einige Pflanzen können Ammonium aufnehmen und verwenden. Jedoch, die meisten bevorzugen Nitrat. In Systemen mit einem Überschuss an Ammonium, die Pflanzen können dazu neigen, länger zu sein und sind oft weniger verkaufsfähig. Auf der anderen Seite, in Systemen mit viel Nitrat, die Probleme mit Blattläusen und anderen Schädlingen können dramatischer sein, mehr Eingriffe erfordern. Seien Sie sich also bewusst, dass Systeme mit zu vielen Nitraten vermehrt Probleme mit Schädlingen haben können.
Auf jeden Fall, das Endprodukt ist Nitrat (NO3-). Einige Pflanzen können Ammonium aufnehmen und verwenden. Jedoch, die meisten bevorzugen Nitrat. In Systemen mit einem Überschuss an Ammonium, die Pflanzen können dazu neigen, länger zu sein und sind oft weniger verkaufsfähig. Auf der anderen Seite, in Systemen mit viel Nitrat, die Probleme mit Blattläusen und anderen Schädlingen können dramatischer sein, mehr Eingriffe erfordern. Seien Sie sich also bewusst, dass Systeme mit zu vielen Nitraten vermehrt Probleme mit Schädlingen haben können.
Nitrat, Nitrit, und Ammoniakwerte können einfach mit einem Süßwasser-Testkit getestet werden, wie dieser. Nitrat löst sich in der Lösung und wird sofort von Bakterien konkurriert, Pilze, Algen und andere Pflanzen. Alle diese Organismen nehmen Nitrat auf und verwenden es in ihren Geweben. Als Bakterien, Pilze, und Algen sterben, dass Stickstoff (oft in Form von Protein) wieder in das System eindringt und der Kreislauf von vorne beginnt. Ein Großteil des Nitrats, jedoch, geliefert wird, gesund und munter, in die Wurzelzone, wo die Pflanzen in Ihrem System es aufnehmen und zum Wachsen verwenden.
Es ist zwar gefährlich, Ammoniak- oder Nitritwerte von weit über 2 ppm bzw. 1 ppm zu haben, Nitrat kann oft weit über 100 ppm liegen (bei vielen Nitrattests weit außerhalb der Tabelle), ohne eine Bedrohung für Ihre Fische darzustellen. Viele hydroponische Systeme verwenden Nitrat im Bereich von 160 ppm. Pflanzen können oft sogar noch höhere Werte schätzen, aber der Aquaponic-Züchter muss ein Gleichgewicht zwischen den Bedürfnissen der Fische finden, die Systemökologie (einschließlich Schädlinge), und die Bedürfnisse der Pflanzen. Aus diesem Grund, Ich empfehle den meisten Aquaponic-Growern, zu schießen, um ihr Nitrat im Bereich von . zu halten 40-80 ppm für immer, gleichmäßiges Pflanzenwachstum.
Viele Systeme haben es schwer, den Stickstoffgehalt aufrechtzuerhalten, vor allem, wenn das System reift, Pflanzen werden groß und die Systemökologie komplexer. Dies kann eine Erhöhung der Fütterung erforderlich machen, um den erhöhten Bedarf zu decken. Viele Leute wollen zunächst die Besatzdichte erhöhen, aber das ist oft ein fehler. Stattdessen, Fütterungsrate erhöhen (aber nicht überfüttern!), und sehen Sie, ob mit der gleichen Menge Fisch höhere Nitratwerte erreicht werden können.

Da Stickstoff ein beweglicher Nährstoff ist (er wird an verschiedene Stellen innerhalb der Pflanze geleitet), Mängel wirken sich zuerst auf das ältere Wachstum aus. Die Symptome eines Mangels sind totale Chlorose ohne Muster auf dem Blatt und verkümmerter Wuchs. Lesen Sie unseren Leitfaden für Anfänger zu Nährstoffmängeln für mehr.
Neben Fischfutter, Stickstoff gelangt durch Düngemittel in das System. Fast alle Düngemittel haben eine NPK-Bewertung, die Ihnen die relative Konzentration von Stickstoff, Phosphor, und Kalium (in dieser Reihenfolge). Für das vegetative Wachstum (das Wachstum von Stängeln, Laub, und Wurzeln), Stickstoff wird mehr benötigt als jeder andere Mineralstoff.
Auf viele Arten, Stickstoff ist der wichtigste Pflanzennährstoff, aber auch das einfachste. Der nächste Nährstoff auf unserer Liste ist Eisen – ein heikler Nährstoff, aber ein wichtiger.





Eine Gesetzeslücke melken, um (fast) Rohmilch an die Massen zu bringen

Warum der Frühling die perfekte Zeit ist, um Hühner zu bekommen!

Best Practices für die Beweidung von Regierungsflächen

Oregano trocknen:Schritt-für-Schritt-Anleitung

Gartenschädlinge - Würmer

Ein Tag im Leben eines Bienenzüchters

Wie man Hühner für hoffrische Eier züchtet
Die Kurzanleitung für Aquaponic Farmer

Was ist Humus im Boden? Formation, Bedeutung und vieles mehr!

6 Arten von Hydroponik-Systemen für die Home-Farming-Einrichtung